Sommaire
1. La concentration dans les calculs de doses
Définition
La concentration est le rapport entre la quantité de soluté et le volume de solution.
| Concentration | = | Quantité de soluté |
| Volume de solution |
Dans les calculs de doses, la concentration s’exprime le plus souvent en pourcentage.
Il y a deux types d'écritures :
- % : pour cent (100)
- ‰ : pour mille (pour 1 000)
- Attention, selon le produit et/ou la prescription, la concentration peut s’exprimer dans d'autres unités :
- mg/ml : milligramme par millilitre
- g/ml : gramme par millilitre
- mg/l : milligramme par litre
- mg/g : milligramme par gramme
- etc…
2. La concentration exprimée en pourcentage
La concentration exprimée en pourcentage correspond au pourcentage de produit actif dissout dans un volume de solution.
Règle
En pharmacologie « % » correspond à « gramme pour cent millilitre ».
Un produit dosé à X % signifie qu'il a X gramme de produit actif pour 100 millilitres de ce produit.
Importe le volume total du produit dosé à X %, il y aura toujours X gramme de produit actif pour 100 ml de ce produit.
Exemple n°1
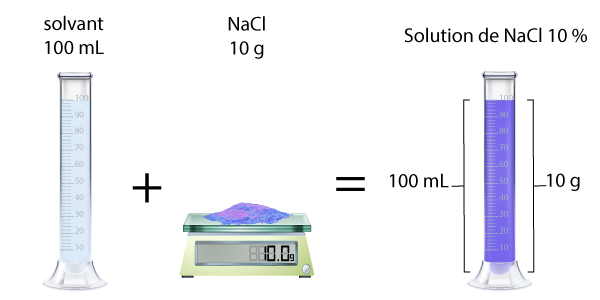
Si on ajoute 10 g de NaCl (chlorure de sodium) dans 100 mL de solvant (eau), on obtient une solution de NaCl dont la concentration est 10 g pour 100 mL, soit 10%.
Exemple n°2
L'ampoule ci-dessous contient une solution de NaCl (chlorure de sodium) qui est dosée à 10 %, ce qui signifie qu'il y 10 g de NaCl dans 100 millilitres de cette solution.
Si cette ampoule ne fait pas 100 mL, mais a un volume de 10 mL, alors, il y a 1 g de NaCl dans 10 mL de cette solution concentrée à 10 %.

Exemple n°3
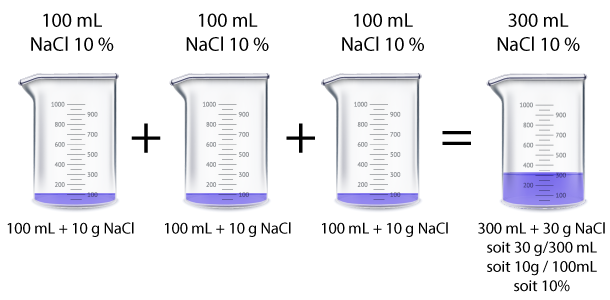
Quelque soit le volume de l'ampoule, il y a aura toujours 10 g de NaCl dans 100 millilitres de solution.
Une solution de 300 mL de NaCl concentrée à 10 %, contient 10 g de NaCl pour chaque 100 millilitres de cette solution.